Antes de comenzar, una aclaración indispensable: no soy médico ni oncólogo; ni siquiera soy enfermero. Soy programador de profesión, investigador curioso por vocación y lector atento de literatura científica, con formación sobre estudios clínicos en el contexto regulatorio de la FDA. Este artículo no pretende indicar tratamientos, dosis ni sustituir el criterio profesional. Lo que hago aquí es comentar algunos artículos y fuentes científicas recientes, tratando de entender qué dicen realmente, qué esperanza abren y cuáles son sus límites.
Ante cualquier diagnóstico de cáncer, el primer camino debe ser siempre el médico tratante, el oncólogo y el equipo de salud.
El cáncer es una palabra que golpea. Cuando aparece en una familia, no solo cambia el cuerpo del paciente: cambia las conversaciones, las prioridades, el calendario, la oración, la esperanza y hasta la forma de mirar el futuro.
Por eso, cuando surge una posible línea de investigación que parece abrir una puerta, es natural querer leer, preguntar y entender. Pero también es indispensable hacerlo con prudencia. La esperanza verdadera no necesita exagerar. Al contrario: se fortalece cuando se apoya en datos, cuando reconoce sus límites y cuando no promete más de lo que la ciencia puede afirmar.
Reposicionamiento de fármacos: una idea legítima
En medicina existe una estrategia conocida como reposicionamiento de fármacos. Consiste en estudiar medicamentos ya conocidos, usados originalmente para una indicación determinada, para explorar si podrían tener utilidad en otras enfermedades.
Esto no es una ocurrencia marginal. Tiene lógica científica: un medicamento ya aprobado suele tener información acumulada sobre seguridad, metabolismo, toxicidad, interacciones y uso humano. Eso no significa que automáticamente sirva para otra enfermedad, pero sí puede justificar nuevas investigaciones.
En ese contexto aparece la ivermectina, un antiparasitario ampliamente conocido. Una revisión publicada en 2021 la describe como un fármaco con potencial anticancerígeno porque distintos estudios de laboratorio han observado que puede interferir con la proliferación de varias células tumorales mediante múltiples vías de señalización.
Una revisión posterior, publicada en 2025, vuelve sobre el tema y analiza sus propiedades químicas, farmacológicas y su potencial terapéutico en oncología. Esa revisión destaca mecanismos moleculares interesantes, pero también advierte que la validación clínica sigue siendo limitada.
¿Qué han encontrado los estudios de laboratorio?
Los estudios revisados describen varios mecanismos por los cuales la ivermectina podría afectar células cancerosas en modelos experimentales.
Entre ellos se mencionan la inducción de apoptosis —muerte celular programada—, alteración de la función mitocondrial, aumento de especies reactivas de oxígeno, interferencia con rutas como Wnt/β-catenina, PI3K/Akt/mTOR, STAT3, PAK1 y YAP1, posible efecto sobre células madre cancerosas, posible reversión de resistencia a ciertos tratamientos y sinergias observadas con algunos medicamentos antitumorales en modelos preclínicos.
Dicho en lenguaje común: algunos experimentos sugieren que la ivermectina podría dificultar ciertos “caminos internos” que la célula tumoral usa para sobrevivir, multiplicarse, resistir medicamentos o escapar de la muerte celular.
Eso es científicamente interesante. Pero no es todavía una prueba clínica.
Una cosa es observar un efecto en una placa de laboratorio o en un modelo animal. Otra muy distinta es lograr ese efecto en un paciente humano, con una dosis segura, una formulación adecuada, distribución real en tejidos, metabolismo individual, interacciones medicamentosas y seguimiento médico.
Un ensayo clínico que merece ser observado
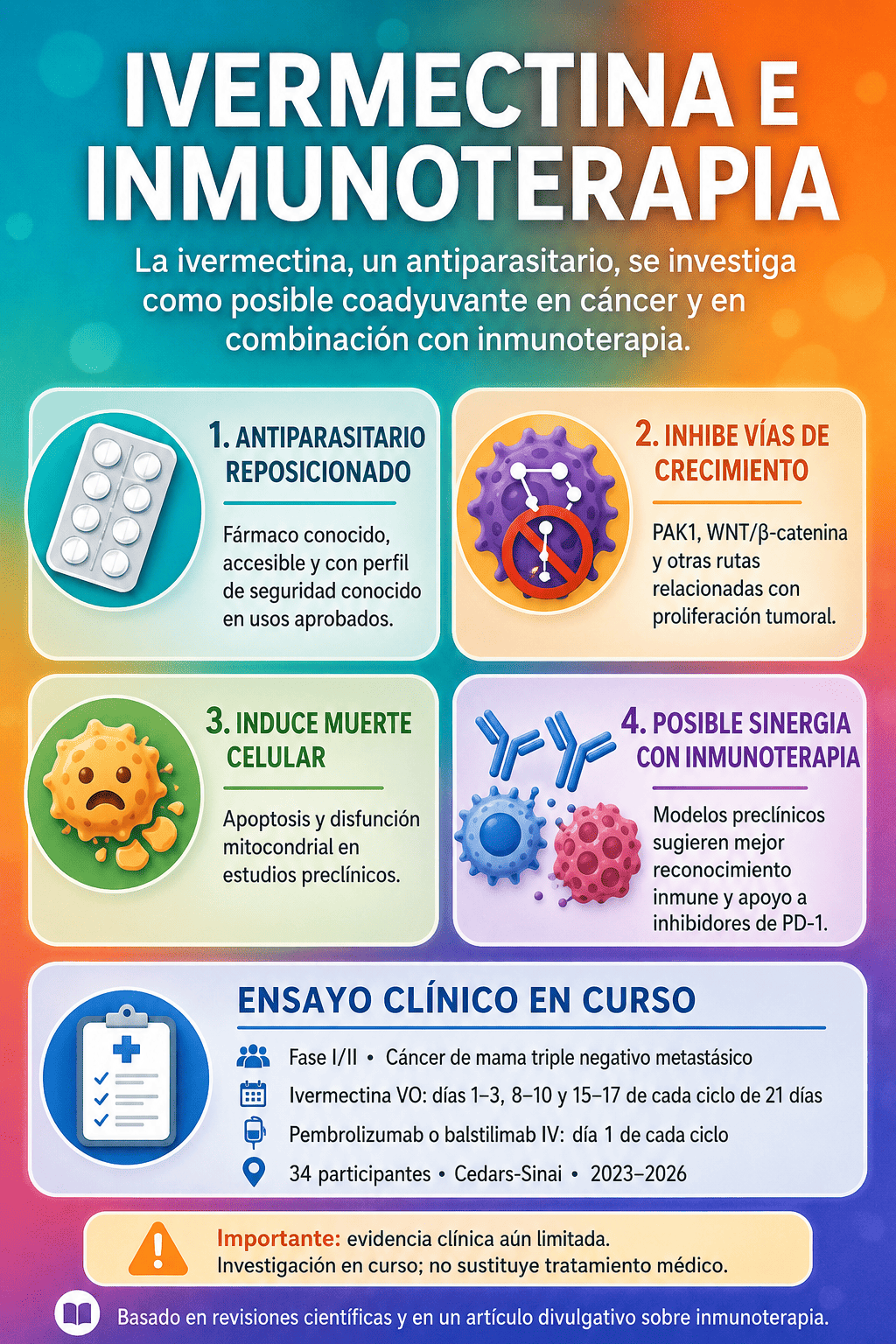
Además de las revisiones científicas sobre ivermectina y cáncer, encontré una fuente divulgativa reciente de OncoDaily que resume un ensayo clínico en curso sobre ivermectina combinada con inmunoterapia en pacientes con cáncer de mama triple negativo metastásico. Este dato es importante porque muestra que el tema ya no está solamente en el terreno de la especulación de internet o de los experimentos aislados de laboratorio: al menos existe una línea clínica formal intentando responder, con método, si esta combinación tiene sentido terapéutico.
El estudio mencionado evalúa la combinación de ivermectina oral con medicamentos de inmunoterapia dirigidos contra PD-1, específicamente pembrolizumab o balstilimab, en pacientes con cáncer de mama triple negativo metastásico. Según el resumen disponible, se trata de un estudio fase I/II, abierto, de un solo brazo, con 34 participantes adultos, realizado en Cedars-Sinai Medical Center, con inicio en octubre de 2023 y finalización estimada para octubre de 2026.
Lo interesante de este ensayo no es que ya demuestre eficacia —porque todavía no la demuestra—, sino la pregunta que está intentando contestar. La hipótesis es que la ivermectina podría ayudar a modificar el microambiente tumoral, favorecer el reconocimiento inmunológico del tumor y, eventualmente, mejorar la respuesta a inhibidores de puntos de control inmunitario como los anti-PD-1.
En palabras más sencillas: algunos tumores son “fríos”, es decir, tienen poca infiltración inmune y responden peor a la inmunoterapia. La pregunta científica es si un medicamento reposicionado podría contribuir a volverlos más “visibles” para el sistema inmune. La misma fuente explica que el interés surge de datos preclínicos donde la ivermectina parece interferir con rutas de crecimiento tumoral, promover muerte celular y mejorar el reconocimiento inmune.
Conviene subrayarlo con fuerza: un ensayo clínico en curso no es una confirmación de eficacia. Es una investigación diseñada para evaluar seguridad, tolerabilidad, dosis y señales iniciales de beneficio. Mientras no existan resultados publicados, revisados y reproducibles, no se puede afirmar que la ivermectina funcione como tratamiento contra el cáncer. Pero sí se puede decir algo esperanzador y prudente: la pregunta es suficientemente seria como para que investigadores la estén evaluando formalmente.
Este estudio también ayuda a entender mejor el tipo de esperanza que deberíamos cultivar. No se trata de automedicarse ni de abandonar tratamientos validados. Se trata de pedir que las hipótesis razonables sean estudiadas con herramientas científicas: protocolos, criterios de inclusión, seguimiento, medición de respuesta tumoral, evaluación de toxicidad y publicación de resultados. Esa es la diferencia entre una promesa peligrosa y una esperanza responsable.
El problema de la dosis y la concentración
Este es uno de los puntos más delicados.
Para usos antiparasitarios reconocidos, la ivermectina se dosifica normalmente en microgramos por kilogramo. Por ejemplo, en distintas indicaciones antiparasitarias se encuentran esquemas cercanos a 150–200 mcg/kg, dependiendo de la enfermedad, la guía clínica y el criterio médico.
Un ejemplo meramente matemático ayuda a entender la escala:
- Persona de 60 kg.
- A 150 mcg/kg: 60 × 150 mcg = 9,000 mcg = 9 mg.
- A 200 mcg/kg: 60 × 200 mcg = 12,000 mcg = 12 mg.
Pero aquí está la advertencia esencial: eso corresponde a usos antiparasitarios, no a un protocolo contra el cáncer.
No existe hoy una dosis oncológica validada de ivermectina. No se puede tomar una dosis antiparasitaria y convertirla, por intuición o por esperanza, en tratamiento anticancerígeno.
La revisión de 2025 muestra precisamente uno de los grandes obstáculos: muchas concentraciones que producen efectos en células tumorales in vitro son mucho más altas que las concentraciones plasmáticas que pueden alcanzarse de forma segura en humanos. En otras palabras: que algo funcione sobre células en laboratorio no significa que pueda lograrse el mismo efecto dentro del cuerpo humano sin toxicidad o sin problemas farmacológicos.
Por eso, si este tema se conversa públicamente, conviene hacerlo así: la ivermectina tiene una historia de uso humano y dosis antiparasitarias conocidas, pero el salto hacia oncología exige ensayos clínicos bien diseñados. Sin esos estudios, hablar de dosis “seguras y eficaces” contra cáncer sería prematuro.
El obstáculo químico: no basta con que algo funcione en laboratorio
El artículo de 2025 insiste en un punto importante: la ivermectina tiene propiedades químicas que dificultan su uso sistémico como posible terapia antitumoral. Es altamente lipofílica y tiene baja solubilidad en agua, lo cual afecta su biodisponibilidad y su distribución en el organismo.

Por eso, parte de la investigación actual explora estrategias como nanoencapsulación, cocristalización y vehículos de liberación que podrían mejorar su solubilidad, estabilidad y llegada a tejidos específicos.
Esto es importante porque el problema no es solo “cuánto tomar”. En farmacología, la pregunta real es mucho más compleja: cuánto llega a la sangre, cuánto llega al tejido tumoral, cuánto permanece activo, cuánto se metaboliza, qué efectos causa en tejidos sanos y cómo interactúa con otros medicamentos.
El artículo retractado del Dr. Makis y el fenbendazol
En este tema aparece con frecuencia el nombre del Dr. William Makis. Es importante mencionarlo, porque muchas personas llegan a estas conversaciones por videos, entrevistas o publicaciones relacionadas con él.
Uno de los artículos más comentados asociados a su nombre fue una serie de casos publicada en 2025 sobre fenbendazol, no ivermectina. El fenbendazol es otro antiparasitario, usado principalmente en medicina veterinaria, perteneciente a la familia de los benzimidazoles. El artículo describía tres pacientes con cáncer avanzado —mama, próstata y melanoma— que se autoadministraron fenbendazol junto con otros tratamientos o suplementos, y reportaba remisiones o respuestas importantes.
Sin embargo, ese artículo aparece marcado como “Retracted Article”, es decir, artículo retractado. Un artículo retractado no debe usarse como evidencia clínica confiable. No significa necesariamente que cada frase sea falsa, pero sí significa que la revista lo retiró formalmente de la literatura científica válida.
También es sano recordar que una retractación no siempre significa que cada dato del artículo sea falso. A veces responde a errores metodológicos, conflictos de interés no declarados, problemas éticos, fallas en la revisión o deficiencias en la forma en que se presentó la información. Por eso, más que usar un artículo retractado como prueba, conviene preguntarse con rigor cuáles fueron las razones concretas de la retractación, leer la nota editorial correspondiente y distinguir entre una hipótesis que merece estudio y una evidencia clínica ya validada.
En temas sensibles, especialmente cuando hay medicamentos baratos, enfermedades graves e intereses económicos enormes, la transparencia es indispensable. Pero la desconfianza no debe sustituir al método científico: si una retractación parece discutible, la respuesta correcta no es convertir el caso en bandera, sino exigir documentación, revisión independiente y ensayos clínicos bien diseñados.
Además, aun antes de considerar la retractación, el propio texto reconocía limitaciones importantes: eran solo tres casos, sin grupo control, con múltiples tratamientos concomitantes, con autoadministración fuera de protocolos regulados y sin capacidad para demostrar causalidad.
Por honestidad intelectual, conviene decirlo claramente: los casos llamativos pueden abrir preguntas, pero no prueban un tratamiento. Pueden justificar investigación, pero no reemplazan un ensayo clínico.
Ivermectina y mebendazol: un preprint observacional que abre otra pregunta
También encontré un preprint publicado en Zenodo en abril de 2026 titulado “Real-World Clinical Outcomes of Ivermectin and Mebendazole in Cancer Patients: Results from a Prospective Observational Cohort”. Es importante subrayar desde el inicio que Zenodo advierte expresamente que los preprints no han sido revisados por pares y deben considerarse preliminares hasta ser evaluados por expertos independientes. Por tanto, este documento no debe leerse como evidencia clínica concluyente, sino como material generador de hipótesis.
El estudio describe una cohorte observacional prospectiva de 197 pacientes con cáncer a quienes se les prescribió, fuera de indicación aprobada, una combinación de ivermectina y mebendazol mediante una plataforma de telemedicina atendida por profesionales licenciados en Estados Unidos. Los participantes recibieron cápsulas compuestas con 25 mg de ivermectina y 250 mg de mebendazol, y los datos se recolectaron mediante encuestas digitales voluntarias al inicio y aproximadamente a los seis meses.
Según el resumen del preprint, de los 197 pacientes iniciales, 122 completaron la encuesta de seguimiento, lo que equivale a una tasa de respuesta de 61.9%. La población era heterogénea: incluía cáncer de próstata, mama, pulmón, colon, cánceres urológicos, pancreáticos, hepáticos, ginecológicos y hematológicos. También se reporta que una proporción relevante de los participantes utilizaba tratamientos convencionales en paralelo, incluyendo quimioterapia, radioterapia o cirugía, además de suplementos y modificaciones dietéticas.
El resultado más llamativo fue una tasa de beneficio clínico reportada del 84.4%, definida como la suma de respuesta completa, respuesta parcial y enfermedad estable sobre el total de pacientes evaluados. Dentro de esos resultados, el documento informa que 15.6% reportó regresión, 32.8% reportó no tener evidencia actual de enfermedad, 36.1% reportó estabilidad de la enfermedad y 15.6% reportó progresión. También se reportaron efectos secundarios leves, principalmente gastrointestinales, en 25.4% de los participantes.
Estos datos son llamativos y, si fueran confirmados en estudios controlados, serían clínicamente relevantes. Pero deben leerse con mucha prudencia. El propio resumen del preprint reconoce limitaciones importantes: diseño observacional, resultados autorreportados por los pacientes, posible sesgo de selección y factores de confusión no controlados. En otras palabras, el estudio no permite afirmar que la combinación ivermectina-mebendazol haya causado directamente los resultados observados.
La limitación más importante es que no se trata de un ensayo aleatorizado, doble ciego y controlado con placebo. Tampoco parece haber una confirmación radiológica uniforme, un grupo comparativo equivalente ni control completo de terapias simultáneas. Cuando hay pacientes con distintos tipos de cáncer, diferentes estadios, tratamientos convencionales concurrentes y datos reportados por encuesta, es muy difícil aislar el efecto real de los medicamentos estudiados.
Con todo, no creo que deba descartarse sin más. Un estudio observacional de este tipo puede servir para algo valioso: señalar que existe una hipótesis que merece evaluación formal. Si una combinación barata, conocida y relativamente accesible muestra una señal de beneficio en datos del mundo real, la respuesta correcta no debería ser proclamar una cura, pero tampoco ignorarla. La respuesta correcta es exigir ensayos clínicos prospectivos, aleatorizados, controlados, con medición objetiva de respuesta tumoral, evaluación de toxicidad, control de tratamientos concomitantes y revisión independiente.
Este preprint refuerza la idea central de este artículo: la esperanza puede ser legítima, pero necesita método. Las señales observacionales pueden abrir preguntas; solo los ensayos clínicos rigurosos pueden convertir una pregunta en conocimiento médico confiable.
Esperanza sí, imprudencia no
La esperanza no debe confundirse con precipitación.
Hay razones legítimas para investigar la ivermectina y otros fármacos reposicionados. Los mecanismos descritos son interesantes. Los estudios preclínicos merecen atención. La posibilidad de encontrar tratamientos accesibles, de bajo costo y con perfiles conocidos de seguridad es una aspiración profundamente humana y científicamente valiosa.
Pero también hay riesgos reales. La automedicación en cáncer puede retrasar tratamientos efectivos, producir interacciones, afectar el hígado, generar falsa seguridad o llevar a decisiones tomadas desde el miedo más que desde la evidencia.
Nadie debería abandonar tratamientos oncológicos validados para sustituirlos por protocolos encontrados en internet. Nadie debería tomar dosis empíricas sin supervisión médica. Nadie debería interpretar un caso exitoso como garantía de resultado.
En medicina, y especialmente en oncología, la diferencia entre una hipótesis prometedora y un tratamiento probado es enorme.
Lo que sí podemos decir hoy
Después de leer estos artículos, creo que se puede decir lo siguiente con prudencia:
- La ivermectina es un medicamento conocido que ha mostrado efectos antitumorales en estudios preclínicos.
- Esos efectos parecen involucrar múltiples rutas celulares relevantes para el cáncer.
- El reposicionamiento de fármacos es una estrategia científica legítima.
- Hay un ensayo clínico en curso que estudia ivermectina combinada con inmunoterapia en cáncer de mama triple negativo metastásico.
- La evidencia clínica en humanos sigue siendo insuficiente.
- No existe una dosis oncológica validada de ivermectina.
- Las dosis antiparasitarias conocidas no deben confundirse con protocolos contra el cáncer.
- Los casos anecdóticos, incluso cuando son esperanzadores, no demuestran causalidad.
- Los artículos retractados pueden mencionarse como contexto, pero no deben usarse como prueba.
- La investigación debe continuar, pero con ensayos clínicos, transparencia, ética y supervisión médica.
Conclusión
La ivermectina no debe ser presentada como cura contra el cáncer. Pero tampoco debería ser descartada sin estudio serio si existen mecanismos biológicos que justifican investigación adicional.
Entre la censura y la propaganda existe un camino mejor: la lectura honesta, la prudencia clínica y la esperanza responsable.
La ciencia avanza haciendo preguntas. Algunas respuestas nacen en el laboratorio, otras se confirman o se descartan en ensayos clínicos. La ivermectina, en oncología, parece estar todavía en ese territorio intermedio: el de una pregunta científica legítima, interesante y esperanzadora, pero aún no resuelta.
Y mientras esa respuesta llega, el paciente merece algo más que promesas: merece verdad, acompañamiento médico, investigación rigurosa y una esperanza que no lo ponga en peligro.
Fuentes consultadas
- Robalino, K. N.; Vivanco-Galván, O.; Romero-Benavides, J. C.; Jiménez-Gaona, Y. “Ivermectin as an Alternative Anticancer Agent: A Review of Its Chemical Properties and Therapeutic Potential.” Pharmaceuticals, 2025.
PDF: https://boletin.info/wp-content/uploads/2026/05/pharmaceuticals-18-01459-v2.pdf - Tang, M. et al. “Ivermectin, a potential anticancer drug derived from an antiparasitic drug.” Pharmacological Research, 2021.
PDF: https://boletin.info/wp-content/uploads/2026/05/1-s2.0-S1043661820315152-main.pdf - Makis, W.; Baghli, I.; Martinez, P. “Fenbendazole as an Anticancer Agent? A Case Series of Self-Administration in Three Patients.” Case Reports in Oncology, 2025. Artículo retractado.
PDF: https://boletin.info/wp-content/uploads/2026/05/000546362.pdf - OncoDaily. “Antiparasitic Drug Ivermectin and Immunotherapy for Cancer Treatment, Evidence and Ongoing Clinical Trials.”
Enlace: https://oncodaily.com/oncolibrary/ivermectin-and-immunotherapy - ClinicalTrials.gov. “Ivermectin in Combination With Balstilimab or Pembrolizumab in Patients With Metastatic Triple Negative Breast Cancer.” NCT05318469.
Enlace: https://clinicaltrials.gov/study/NCT05318469 - Hulscher, N. et al. “Real-World Clinical Outcomes of Ivermectin and Mebendazole in Cancer Patients: Results from a Prospective Observational Cohort.” Preprint, Zenodo, 2026. Enlace: https://zenodo.org/records/19455636